Vous êtes ici
TROD INSTI : Etudes de validation
Dépistage du VIH au sein des salons régionaux de l’érotisme : une approche française novatrice
Télécharger la notice d'utilisation du TROD INSTI® VHC
Télécharger la présentation TROD INSTI® VHC
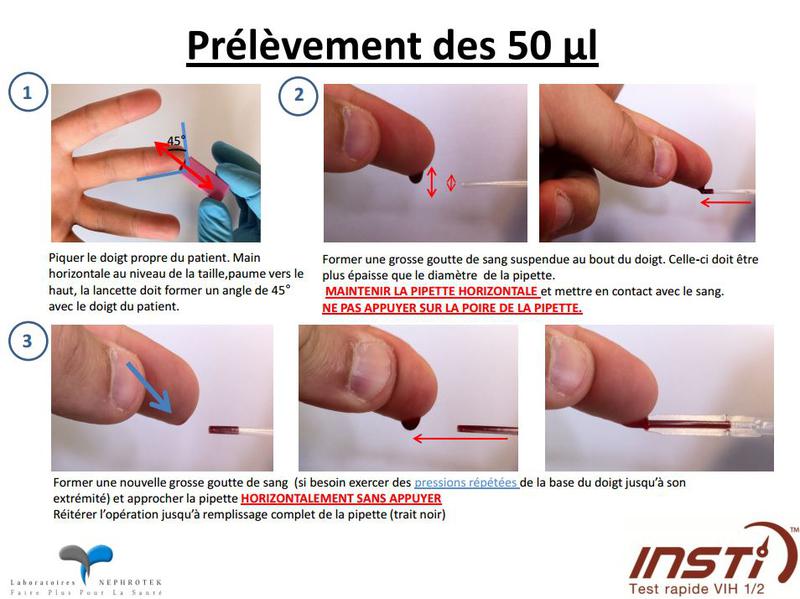
Télécharger la procédure de prélèvement
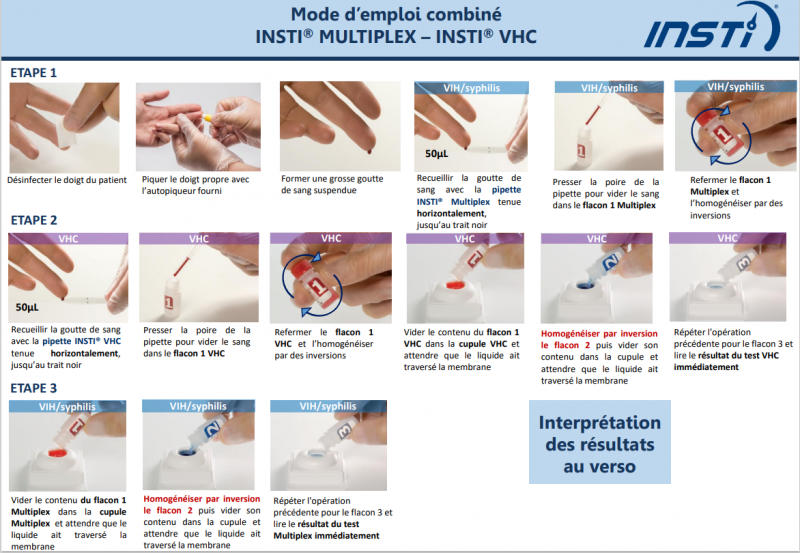
Télécharger le protocole combiné INSTI® MULTIPLEX / INSTI® VHC
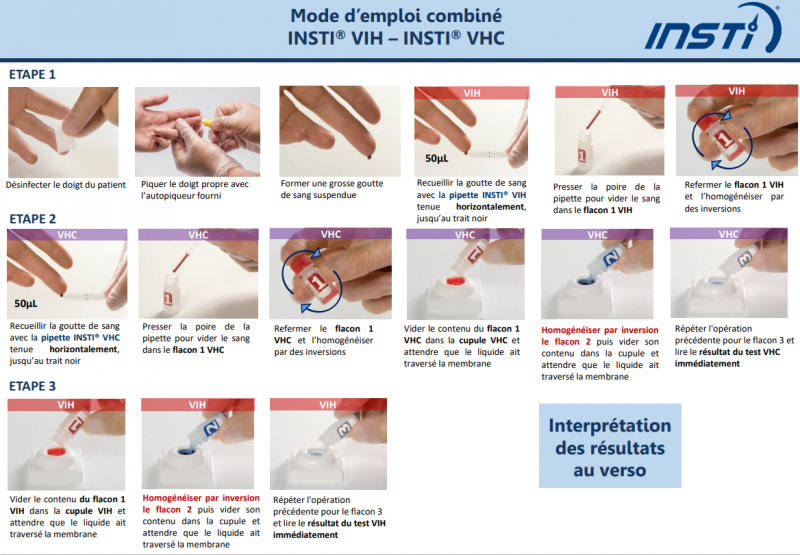
Télécharger le protocole combiné INSTI® VIH / INSTI® VHC
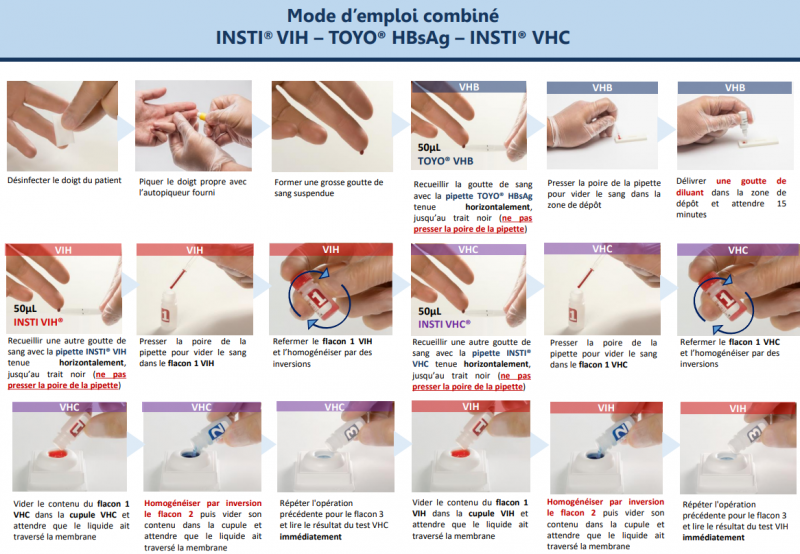
Télécharger le protocole combiné INSTI® VIH / TOYO® VHB / INSTI® VHC
*TROD : Test Rapide d’Orientation Diagnostique
(1) p.58 du rapport de la Haute Autorité de Santé (HAS) sur la « Place des tests rapides d’orientation diagnostique (TROD) dans la stratégie de dépistage de l’hépatite C ». http://www.has-sante.fr/portail/jcms/c_1743868/fr/depistage-de-lhepatite-c-la-haute-autorite-de-sante-se-prononce-en-faveur-des-tests-rapides-dorientation-diagnostique-trod
(2) p.125 du rapport de recommandations 2014 sous la direction du Pr Dhumeaux sur la « Prise en charge des personnes infectées par les virus de l’hépatite B ou de l’hépatite C ». http://www.sante.gouv.fr/journee-nationale-de-lutte-contre-les-hepatites-b-et-c-19-mai-2014.html
Nom du produit : | INSTITM VHC |
|
Conditionnement : | Test unitaire | |
Type de diagnostic : | Recherche des anticorps anti-VHC | |
Nature du prélèvement : | Sang total capillaire, sang total veineux/EDTA, sérum, plasma | |
Technique : | Immunofiltration sur membrane | |
Stockage : | entre 2°C et 30°C | |
Volume d'échantillon nécessaire : | 50 µL | |
Lecture : | Immédiate | |
Nécessité de matériel complémentaire : | Aucun (accessoires de prélèvement inclus) | |
Contrôle interne : | Réel contrôle immunologique (protéine A/IgG) | |

Abstract:
Background: Anti-HIV-1 IgM antibody is an important immunoassay target for early HIV antibody detec-tion.Objectives: The objective of this study is to determine if the early HIV antibody sensitivity of the 60 s INSTItest is due to detection of anti-HIV-1 IgM in addition to IgG.Study Design: To demonstrate HIV gp41 IgM antibody capture by the INSTI HIV-1 gp41 recombinant anti-gen, an HIV-IgM ELISA was conducted with commercial HIV-1 seroconversion samples. To demonstratethat the INSTI dye-labelled Protein A-based colour developer (CD) has affinity to human IgM, commercialpreparations of purified human immunoglobulins (IgM, IgD, IgA, IgE, and IgG) were blotted onto nitro-cellulose (NC) and probed with the CD to observe spot development. To determine that INSTI is able todetect anti-HIV-1 IgM antibody, early seroconversion samples, were tested for reduced INSTI test spotintensity following IgM removal.Results: The gp41-based HIV-IgM ELISA results for 6 early seroconversion samples that were INSTI positivedetermined that the assay signal was due to anti-HIV-1 IgM antibody capture by the immobilised gp41antigen. The dye-labelled Protein-A used in the INSTI CD produced distinct spots for purified IgM, IgA, andIgG blotted on the NC membrane. Following IgM removal from 21HIV-1 positive seroconversion sampleswith known or undetermined anti-HIV-1 IgM levels that were western blot negative or indeterminate,all samples had significantly reduced INSTI test spot intensity.Conclusions: The INSTI HIV-1/HIV-2 Antibody Test is shown to detect anti-HIV-1 IgM antibodies in earlyHIV infection which enhances its utility in early HIV diagnosis.
Télécharger l'étude
Résumé :
Les tests rapides d’orientation et de diagnostic (TROD) VIH sont recommandés dans le dépistage de l’infection VIH « hors les murs ». Leur utilisation en CDAG/CDDIST peut favoriser la demande mais pourrait affecter le rendu des résultats des autres tests réalisés de manière concomitante, dans la mesure où celui-ci est plus tardif.
Les objectifs de cette étude étaient : i) mesurer l’impact de l’introduction des TROD sur le rendu des résultats des autres infections dépistées et ii) mesurer l’impact de la mise en place de mesures de rappel téléphonique (envoi de SMS ou appel) des consultants sur le nombre de résultats non rendus après réalisation d’un TROD VIH. Ce travail a débuté en avril 2011 et s’est déroulé sur 15 mois, en deux phases successives, dans les CDAG/CDDIST d’Orléans et de Blois.
Durant la première phase, les TROD et des tests Elisa ont été proposés une semaine sur deux. Au total, 445 personnes ont été incluses (197 TROD ; 248 Elisa). Le taux de perdus de vue (PDV) pour le rendu du résultat VIH était significativement plus faible parmi les patients ayant bénéficié d’un TROD (0%) que parmi les patients ayant bénéficié d’une sérologie VIH classique (7,3%) (p<0,001), alors que le taux de PDV pour la remise des résultats des tests autres que celui du VIH était significativement plus élevé parmi les patients ayant bénéficié d’un TROD (19,8% versus 13,2% ; p=0,05).
Au cours de la seconde phase, un appel téléphonique direct au consultant, en cas de non-retour après un TROD, a permis de réduire le taux de PDV pour les autres sérologies à 10,2%.
L’utilisation des TROD en CDAG/CDDIST favorise l’accès au dépistage. Cependant, lorsque des tests de dépistage non rapides doivent être réalisés de manière concomitante, des mesures de rattrapage des consultants perdus de vue doivent être mise en oeuvre.
- Etude comparative de 6 tests rapides sur un panel de 200 personnes séropositives sur sang capillaire, sérum et salive.
- Conclusions : le TROD INSTI présente la meilleure sensibilité sur sang capillaire (99,00% avec séroconversion, 99,5% hors séroconversion). INSTI est le seul test à détecter une des deux séroconversions en l’absence de détection d’antigène p24 dans le kit. INSTI est le seul test avec une sensibilité équivalente sur sang capillaire et sérum.
Introduction – objectifs : Le vaccin antiamaril (VAA), vaccin vivant atténué recommandé en zone d’endémie de la fièvre jaune d'Afrique sub-saharienne et d'Amérique du Sud, est contre-indiqué au cours de l’infection par le VIH avec déficit immunitaire sévère (CD4<200/mm3) ou symptomatique. La faisabilité et l’acceptabilité de la proposition systématique d’un test de dépistage rapide de l’infection par le VIH (TROD) avant VAA a été évaluée.
Matériels et méthodes : Une proposition systématique de TROD a été faite dans 4 centres de vaccination internationale (CVI) à tous les sujets adultes candidats au VAA dont l’infection par le VIH était inconnue. Dans 3 des 4 CVI, les TROD et le conseil ont été réalisés par des associatifs formés et accrédités.
Résultats : Parmi les 1256 sujets éligibles, 255 tests ont été proposés et 153 TROD ont été réalisés, tous négatifs, soit un taux de faisabilité global de 12,2% (153/1256). Dans les centres ayant bénéficié de l’intervention des associations, le taux de faisabilité est de 54,1% (106/196 TROD faits), ce taux baisse à 4,4% (47/1060) en l’absence d’aide. Le taux d’acceptabilité global est de 60% (153/255 TROD acceptés), l’acceptation diminuant avec l’âge. Soixante pour cent des voyageurs disent avoir déjà eu d’un test de dépistage, majoritairement entre 1 et 5 ans plus tôt, et 22.5% de ceux qui refusent le TROD n’ont jamais été dépistés (28/102). Cette action est jugée comme plutôt ou tout à fait satisfaisante par 97,7% (85/87) des voyageurs interrogés après avoir été dépistés.
Conclusion : La proposition de TROD avant VAA est bien acceptée par les voyageurs et sa faisabilité peut être améliorée avec le soutien logistique des associations.